Khoa học tự nhiên 8 (Kết nối tri thức với cuộc sống)
-
Chương I. Phản ứng hoá học
Bài 2. Phản ứng hoá học3 Topics|1 Quiz -
Bài 3. Mol và tỉ khối chất khí5 Topics|4 Quizzes
-
Bài 4. Dung dịch và nồng độ5 Topics|4 Quizzes
-
Bài 5. Định luật bảo toàn khối lượng và phương trình hoá học6 Topics|5 Quizzes
-
Bài 6. Tính theo phương trình hoá học4 Topics|4 Quizzes
-
Bài 7. Tốc độ phản ứng và chất xúc tác2 Topics|1 Quiz
-
Chương II. Một số hợp chất thông dụngBài 8. Acid2 Topics|1 Quiz
-
Bài 9. Base. Thang pH3 Topics|1 Quiz
-
Bài 10. Oxide3 Topics|1 Quiz
-
Bài 11. Muối3 Topics|1 Quiz
-
Bài 12. Phân bón hoá học2 Topics|1 Quiz
-
Chương III. Khối lượng riêng và áp suấtBài 13. Khối lượng riêng1 Topic
-
Bài 14. Thực hành xác định khối lượng riêng1 Topic
-
Bài 15. Áp suất trên một bề mặt1 Topic
-
Bài 16. Áp suất chất lỏng. Áp suất khí quyển2 Topics
-
Bài 17. Lực đẩy Archimedes1 Topic
-
Chương IV. Tác dụng làm quay của lựcBài 18. Tác dụng làm quay của lực. Moment lực2 Topics
-
Bài 19. Đòn bẩy và ứng dụng2 Topics
I. ĐỊNH NGHĨA
– Phản ứng hóa học là quá trình biến đổi từ chất này sang chất khác.
– Chất ban đầu bị biến đổi trong phản ứng gọi là chất phản ứng hay chất tham gia.
– Chất mới sinh ra gọi là sản phẩm.
– Phương trình chữ của phản ứng hóa học: Tên các chất tham gia → Tên các sản phẩm
– Cách đọc phương trình chữ của phản ứng hóa học:
+ Dấu “+” ở trước phản ứng đọc là “tác dụng với” hay “phản ứng với”
+ Dấu “+” sau phản ứng đọc là “và”
+ Dấu “→” đọc là “tạo thành” hay “tạo ra” hoặc “phân hủy ra”
– Trong quá trình phản ứng lượng chất tham gia giảm dần còn lượng chất sản phẩm tăng dần.
Ví dụ 1: Hãy đọc các phương trình chữ sau:
a) Sắt + lưu huỳnh → Sắt (II) sunfua.
“Sắt tác dụng với lưu huỳnh tạo thành sắt hai sunfua”
b) Đường → nước + than
“Đường phân hủy thành nước và than”
c) Than + oxi → khí cacbonic
“Than phản ứng với oxi tạo thành khí cacbonic”
d) Kẽm + axit → Kẽm clorua + khí hiđro
“Kẽm tác dụng với axit tạo ra kẽm clorua và khí hiđro”
Ví dụ 2: Hãy viết phương trình chữ khi cây nến cháy (biết nến là parafin) tạo ra khí cacbonic và nước
Hướng dẫn: Parafin + oxi → cacbonic + nước
2. DIỄN BIẾN CỦA PHẢN ỨNG HÓA HỌC
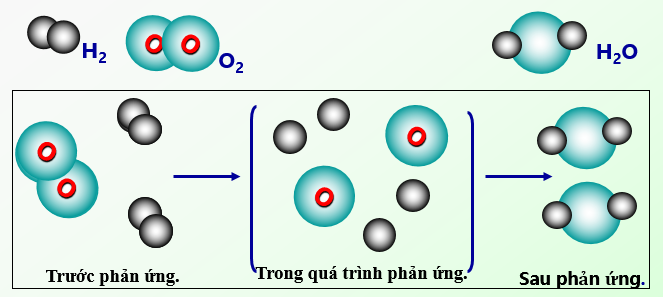
Kết luận:
– Trong các phản ứng hóa học, chỉ có liên kết giữa các nguyên tử thay đổi làm cho phân tử này biến đổi thành phân tử khác.
Lưu ý:
+ Nếu có đơn chất kim loại tham gia phản ứng thì sau phản ứng nguyên tử kim loại phải liên kết với nguyên tử của nguyên tố khác.
+ Nếu đơn chất là kim loại thì nguyên tử kim loại sẽ tham gia phản ứng.
3. ĐIỀU KIỆN ĐỂ CÓ PHẢN ỨNG HÓA HỌC XẢY RA
– Các chất tham phản ứng phải được tiếp xúc với nhau.
– Tùy mỗi phản ứng cụ thể mà cần đun nóng đến một nhiệt độ nào đó
Ví dụ: Phản ứng cháy của than, ban đầu cần cung cấp 1 nhiệt độ nhất định mới xảy ra phản ứng. Hoặc phản ứng không cần đun nóng như thả viên kẽm vào dung dịch axit clohiđric.
– Có những phản ứng cần xúc tác thích hợp, đó là chất kích thích cho phản ứng xảy ra nhanh hơn và giữ nguyên không biến đổi khi phản ứng kết thúc.
Ví dụ: Trong quá trình nấu rượu, người ta cho men rượu vào gạo để làm chất xúc tác cho quá trình tạo thành rượu được nhanh hơn.
4. DẤU HIỆU CÓ THỂ NHẬN BIẾT PHẢN ỨNG HÓA HỌC XẢY RA
– Có thể thay đổi màu sắc, trạng thái, mùi.
– Tỏa nhiệt, thu nhiệt hoặc phát sáng.
– Tạo ra kết tủa, bay hơi, hoặc đổi màu

